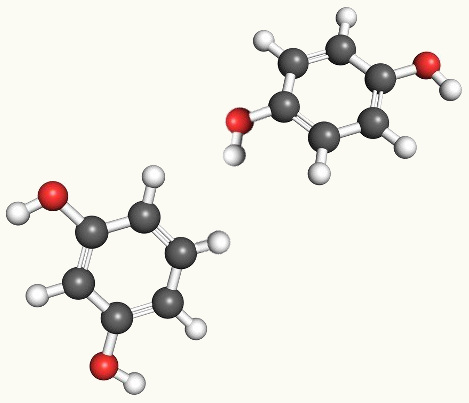
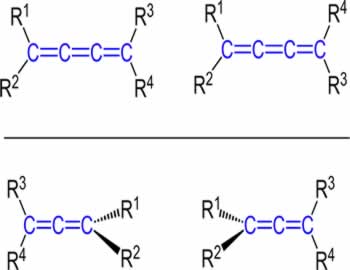
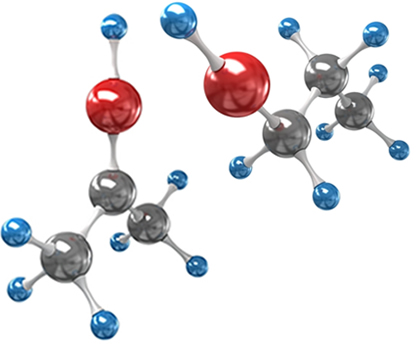
| Isomeria é um fenômeno no qual dois ou mais compostos diferentes possuem a mesma fórmula molecular; porém, fórmulas estruturais diferentes. |
Existem dois tipos de isomeria: a isomeria plana e a espacial (estereoisomeria). Nesse momento, detalharemos a isomeria plana.
| Na isomeria plana pode-se perceber a diferença existente entre um isômero e outro através das suas fórmulas estruturais planas. |
O estudo da isomeria plana é divido em isomeria de função, de cadeia, de posição e de compensação. Observe do que se trata cada uma delas:
1. Isomeria de função ou funcional:
A diferença se encontra no grupo funcional. Por exemplo, nos casos abaixo, ambos os compostos possuem a mesma fórmula molecular, C3H6O2, porém eles são de grupos funcionais diferentes: um é ácido carboxílico e o outro é um éster:
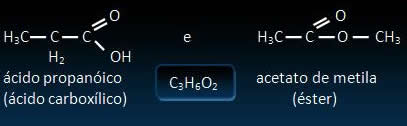
1.1. Tautomeria (isomeria dinâmica):
A tautomeria (tautos = dois de si) é um tipo particular de isomeria de função, pois os isômeros coexistem em equilíbrio dinâmico em solução. Ela ocorre em compostos que apresentam o nitrogênio ou o oxigênio (que são elementos eletronegativos), ligados ao mesmo tempo a um hidrogênio e a um carbono saturado. A alta eletronegatividade desses elementos atrai os elétrons da ligação dupla e a desloca.
Existem dois tipos de tautomeria:
1.1.1. Tautomeria aldoenólica (enol ↔aldeído)

1.1.2. Tautomeria cetoenólica (enol ↔ cetona)

2. Isomeria de cadeia (núcleo ou isomeria constitucional):
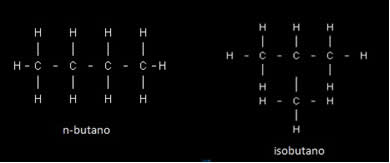
Ambos os compostos pertencem ao mesmo grupo funcional, porém sua diferença se se encontra no seu tipo de cadeia. Por exemplo, na figura abaixo, ambos os compostos são hidrocarbonetos e sua fórmula molecular é C4H10, porém uma cadeia é normal e a outra é ramificada:
3. Isomeria de posição ou posicional:
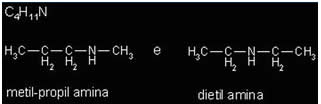
Os seus isômeros se diferenciam quanto à posição de um grupo funcional, de uma ramificação ou de uma instauração. No exemplo a seguir, o grupo funcional (amina) está em posições diferentes:
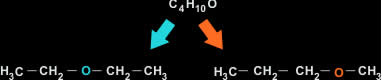
4. Isomeria de compensação (metameria):
A diferença se encontra na posição do heteroátomo dentro da cadeia carbônica: