Os conhecimentos químicos são aplicados em várias situações do nosso cotidiano, e, em algumas, nós nem percebemos. Um exemplo disso é o uso da panela de pressão quando queremos que determinados alimentos, tais como o feijão, cozinhem mais rápido. Mas por que os alimentos na panela de pressão cozinham mais depressa?
Isso acontece porque a panela de pressão possui uma borracha entre a tampa e a panela que a deixa hermeticamente fechada, o que significa que o vapor formado fica aprisionado dentro dela, aumentando a pressão. O aumento da pressão faz com que a água demore mais para entrar em ebulição, atingindo temperaturas mais elevadas que cozinham mais rápido o alimento.
Você já deve ter reparado que, quando colocamos a água para ferver em uma panela aberta, primeiro se formam bolhas no fundo dela, que, com o aumento da temperatura, passam a subir até que todo o líquido entre em ebulição. Isso ocorre porque essas bolhas são formadas por vapor de água. No entanto, existe a pressão atmosférica externa que exerce uma força para baixo, e como a pressão do vapor dentro da bolha inicialmente é menor que a pressão atmosférica, a bolha fica no fundo da panela. Com o aumento da temperatura, a pressão do vapor vai crescendo até que fica igual à pressão atmosférica e, por isso, as bolhas sobem e liberam o vapor de água para o ar.
.jpg)
Ao nível do mar (altitude igual a zero), a pressão atmosférica é igual a 1 atm ou 760 mmHg. Nessas condições, a água entra em ebulição em 100ºC, o que significa que nessa temperatura a pressão de vapor se iguala à pressão atmosférica. No entanto, em lugares em que a pressão é maior, como em lugares de menor altitude, o vapor de água precisará receber mais energia, por atingir valores de temperatura maior até vencer a pressão atmosférica e entrar em ebulição.
Por exemplo, o Mar Cáspio é um mar interior da Ásia que tem altitude de 28 metros abaixo do nível do mar. Nesse lugar, a água ferve a uma temperatura acima de 100°C.
O mesmo ocorre dentro da panela de pressão: visto que a pressão é maior, o líquido precisa receber mais energia para vencê-la e assim entrar em ebulição, o que significa que ele demora mais para passar para o estado de vapor, sua temperatura de ebulição é maior e ele permanece líquido em temperaturas muito maiores.
Para se ter uma ideia, calcula-se que os valores das pressões atingidas dentro da panela de pressão sejam entre 1,4 a 2,0 atm, o que significa que a temperatura interna da panela atinge valores de cerca de 120 ºC. Com uma temperatura muito maior, a comida fica pronta bem mais rápido também.
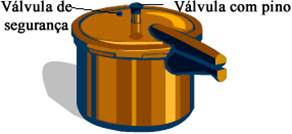
Mas a pressão atinge um valor determinado e estabiliza-se, sendo que o excesso é liberado pela válvula com pino. Isso é importante porque se a pressão interna continuasse a aumentar, a panela explodiria, podendo causar sérios acidentes.
Por segurança, a panela ainda conta com uma válvula de segurança na tampa, que geralmente é uma espécie de borracha vermelha, que só abre em situações extremas, como quando fica algum alimento preso na válvula de pino, impedindo que o vapor seja liberado. Por isso, é muito importante sempre que lavar a panela de pressão, limpar bem a válvula de pino, de preferência passando um palito de dente no furo para retirar qualquer vestígio de comida.