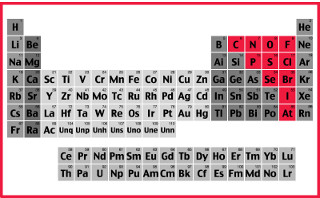
Uma das formas em que os elementos químicos são classificados na Tabela Periódica é dividindo-os em cinco grupos de acordo com as suas propriedades físicas e químicas. A seguir, temos como é feita essa classificação em: hidrogênio, semimetais, ametais, gases nobres e metais.
.jpg)
- Hidrogênio: Esse elemento, que é o mais abundante no Universo, é diferente de todos os outros elementos da Tabela Periódica e se encontra na família 1 (metais alcalinos) porque possui apenas uma camada eletrônica com um elétron nela, mas não compartilha de propriedades semelhantes com os outros elementos desse grupo.
Ele tem a capacidade de se combinar com metais, semimetais e ametais. Além disso, é um gás extremamente inflamável à temperatura ambiente. Quando liquefeito, é usado como combustível de foguetes e, quando comprimido a pressões na ordem de 2,5 milhões de atmosferas, ele pode se tornar metálico, atuando como um supercondutor.

- Metais: Dois terços dos elementos químicos até então descobertos são metais, ou seja, dos 115 elementos existentes, 86 são metais. Veja algumas de suas propriedades principais:
-Todos os elementos desse grupo, com exceção do mercúrio (Hg), são sólidos a temperatura ambiente e, em geral, são duros;
-Eles possuem um brilho metálico característico dos metais;
- São bons condutores de eletricidade e de calor;
-São densos;
- Possuem pontos de fusão e ebulição altos;
-São maleáveis, podendo ser transformados em lâminas;
- São dúcteis, podendo ser transformados em fios, como os fios de cobre usados para conduzir eletricidade;
-Os metais são amplamente utilizados em nossa sociedade, como na produção de joias, moedas, fios elétricos, panelas, talheres, na produção de ligas metálicas como o aço, em decorações de edifícios e de lojas, caldeiras, reatores industriais, cabos de elevadores etc.

- Semimetais: Esses elementos são apenas sete (boro (B), silício (Si), germânio (Ge), arsênio (As), antimônio (Sb), telúrio (Te) e polônio (Po)). Eles são assim chamados porque apresentam propriedades intermediárias entre os metais e os ametais:
-Apresentam brilho metálico como os metais;
-Sua condutibilidade elétrica e térmica é pequena;
-Não são maleáveis, mas fragmentam-se como os ametais;
-Alguns semimetais, como o silício, são usados na fabricação de transistores, de chips e de células solares.

Obs.: A classificação dos elementos em semimetais está em desuso, assim, muitas Tabelas Periódicas trazem apenas metais e ametais. Segundo esse tipo de classificação, o boro, o silício, o arsênio e o telúrio são ametais; enquanto o germânio, o antimônio e o polônio são classificados como metais.
Apesar disso, a IUPAC recomenda que os elementos sejam classificados como metais, semimetais e não metais.
- Ametais: Correspondem a onze elementos químicos (carbono (C), nitrogênio (N), fósforo (P), oxigênio (O), enxofre (S), selênio (Se), flúor (F), cloro (Cl), bromo (Br), iodo (I) e astato (At)). Suas propriedades físicas e químicas são exatamente o oposto das propriedades dos metais:
-Não possuem umbrilho metálico, com exceção do iodo e do carbono na forma de grafite;
- São isolantes térmicos, não sendo condutores de calor e nem de eletricidade;
-A maioria está no estado gasoso à temperatura ambiente;
- Possuempontos de fusão e ebulição baixos;
-Fragmentam-se;
-São usados na fabricação de pneus, para se produzir pólvora, entre outras finalidades.

- Gases Nobres: Esses são os sete elementos pertencentes à família 18 da Tabela Periódica (hélio (He), neônio (Ne), argônio (Ar), criptônio (Kr), xenônio (Xe) e radônio (Rn)).
Esses elementos são colocados num grupo à parte porque eles são bastante estáveis, sendo os únicos elementos químicos que ocorrem na natureza na forma isolada. Eles possuem pouquíssima afinidade com outros elementos químicos, não tendo a tendência de doar nem receber elétrons. Mas, ainda assim, existem alguns compostos de gases nobres feitos em laboratório.